孙炳峰,林国强.天然产物与药物化学概述[J].中国科学院院刊,2011,(Z1):125-133.
天然产物与药物化学概述
Natural Products and Medicinal Chemistry: A Review
天然产物与药物化学概述
Natural Products and Medicinal Chemistry: A Review
作者
孙炳峰
中国科学院上海有机化学研究所 上海 200032
Sun Bingfeng
Shanghai Institute of Organic Chemistry,CAS 200032 Shanghai
林国强
中国科学院上海有机化学研究所 上海 200032
Lin Guoqiang
Shanghai Institute of Organic Chemistry,CAS 200032 Shanghai
中国科学院上海有机化学研究所 上海 200032
Sun Bingfeng
Shanghai Institute of Organic Chemistry,CAS 200032 Shanghai
林国强
中国科学院上海有机化学研究所 上海 200032
Lin Guoqiang
Shanghai Institute of Organic Chemistry,CAS 200032 Shanghai
中文关键词
天然产物,药物化学,有机合成,生物多样性
英文关键词
natural products, medicinal chemistry, organic syntheses, biological diversity
中文摘要
天然产物是大自然对人类的馈赠,为人类的健康幸福发挥着不可替代的作用。现有的化学药物超过半数发源于天然产物,而抗癌药物中更有超过三分之二发源于天然产物。本文通过青蒿素、喜树碱、紫杉醇等药物的研究概况阐述了天然产物在药物发现中的重要性。相关研究需要天然产物化学、有机合成、药物化学等多学科的发展,并在根本上要求维持生物多样性。
英文摘要
Natural products constitute an invaluable resource benefiting the human beings. While their rich structural diversity and complexity continuously appeal the synthetic chemists to generate them artificially, thus advancing the discipline and practice of synthetic chemistry, their diverse bioactivities have made them the origin of over half of the drugs used today. In this paper, three relevant examples were highlighted to illustrate the significance of natural products for drug discovery.
1 药物与药物化学
人类社会发展到今天,大众健康已受到高度重视。大众健康水平关系民众的生活水平,体现社会的发展水平,反映一个国家的综合实力。要维持较高的大众健康水平,不仅要倡导民众保持健康的生活方式,还需要拥有发达完备的医疗系统,而这其中,药物占有关键地位。药物的获得依赖于药物化学的研究,因此药物化学作为一门学科关系到国计民生,具有战略意义[1]。
药物化学 (Medicinal Chemistry) 是关于药物的发现、发展、鉴定和制备,并在分子水平上研究其生理作用的科学,其终极目标是开发出可临床安全应用的药物,服务于人类的健康需求。作为化学和生命科学的交叉学科,药物化学以化学(特别是有机化学)为基础,涉及生物学、医学和药学等多个学科内容,是一门综合性极强的学科[2]。虽然药物化学仅有一个多世纪的学科历史,但人类在药物化学方面的实践却已长达数千年。
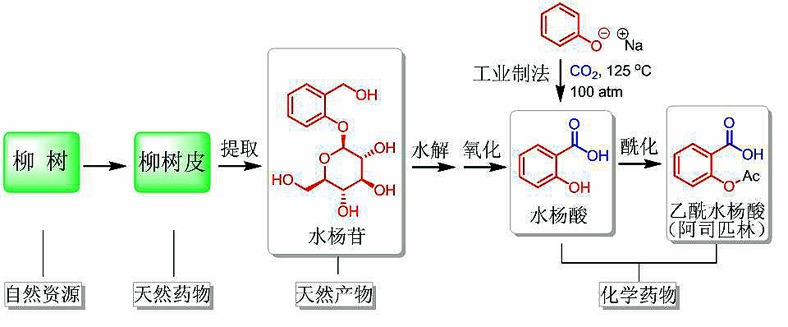
药物按照组成和性质的不同可以分为天然药物,化学药物以及生物药物。人类最早使用的药物是天然药物,包括自然界的一些矿物质,植物的叶、皮、茎、根、籽各部,以及动物的甲壳、骨骼、脏器、分泌物等。早期世界各民族的传统药物,比如中草药、印度草药、地中海草药、非洲草药、南美草药等,均属天然药物。在现代医药发端以前,人类利用天然药物干预疾病已有长达数千年的历史,发现了不少有确切疗效的天然药物。随着科学的发展,19世纪人们就已经认识到,天然药物中所含有的活性化学物质是疗效的物质基础。从药物化学角度看,天然药物的化学成分复杂,常含有上百种化合物;一些天然药物与期望的疗效有差距,或虽有一定疗效但效果不理想,或虽有疗效但毒副作用明显,甚至有害无益。从世界范围来看,虽然在历史上和现实中天然药物已经发挥并仍然在发挥一定作用,但是已经不能满足现代人类对更高品质药物的需求。尽管如此,天然药物这一宝库依然蕴含着不少精华,如能去伪存真、去粗取精获得活性物质,仍然可为药物发现所用[3]。事实上,早期的药物发现几乎都来自于对天然药物活性成分的研究。譬如,阿司匹林的发现就源于对柳树皮活性成分的研究。
公元前5世纪,古希腊名医希波克拉底 (Hippocrates) 记载了咀嚼柳树皮可止痛退烧。柳树皮作为天然药物在西方社会沿用了上千年,在中东、北美民族中也有类似实践。19世纪,随着现代科学的发展,化学家已经具备了从自然界分离出天然产物单体(单一化合物)的手段。1828年,德国人Buchner从柳树皮中分离出水杨苷。1838年意大利人Piria将水杨苷水解并将水解产物氧化得到活性物质水杨酸。1859年德国著名有机化学家Kolbe发明了水杨酸的工业制法。1897年,拜耳公司的Hoffmann制得 乙酰水杨酸纯品,该公司研究用其替代水杨酸,因为水杨酸具有较强刺激性,而乙酰水杨酸要温和得多。1899年,拜耳公司将乙酰水杨酸冠以阿司匹林这一商标名,随后将其推向世界市场(图1)[4]。
与天然药物成分复杂、疗效不确定或不稳定形成鲜明对比,化学药物的组分相对单纯(一般为单一化合物,也有用复方的),疗效确切。从来源考虑,化学药物既可以是从自然界分离得到的天然产物或对其结构改造后的化合物,也可以是通过人工合成或发酵得到的化合物。理想的药物应该在具有疗效的同时没有毒性。然而,古人讲“是药三分毒”,就辩证地指出了药物的两面性,即在产生疗效的同时也具有一定毒副作用。在现代药物化学的研究中,人们以具有活性的天然产物或合成分子为先导化合物(lead compound),通过结构??活性关系 (structure-activity relationship, SAR)研究,获得疗效最大化、毒性最小化的适合临床安全使用的药物。当今,化学药物因在疗效和安全性两方面均远优于天然药物而成为临床应用中最主要使用的药物。在2009年发布的WHO基本药物目录中化学药物占90%以上,其余为生物药物[5]。
药物化学研究的对象就是化学药物,其过程一般包括如下3个阶段:(1)先导化合物的发现与确认;(2)基于SAR的先导化合物的结构优化,临床前及临床研究;(3)规模化生产工艺的建立以及剂型确定等。其中,先导化合物的发现与确认是药物发现之旅的第一步,即针对某一靶标或活性需求进行化合物筛选,发现先导化合物并确定结构。随着高通量筛选技术的建立,人们可在较短时间内对包含成千上万个成员的化合物库进行活性筛选。因此,化合物库的质量和数量就成为高通量筛选有效性的决定性因素。
用于筛选的化合物库内样品主要有人工合成和天然产物两个来源。近年来组合化学 (Combinatory Chemistry)的发展为人工合成化合物数量的快速大量增长提供了新手段。组合化学的基本原理是利用已知的化学反应,对选取的多种分子母核进行多位点的多样化改造,一次操作就可以产生大量的新化合物。这种方法在化合物的结构改造和优化方面具有强大优势,但是,由于该方法是基于母核结构的改造,而母核结构类型事先已定,因此所产生的大量化合物在结构多样性方面有缺陷,因而成药的命中率低,且结构的相对简单导致作用位点的不专一及由此产生的毒副作用[6] 。据Newman等人的调查,完全基于组合化学的原创性的药物仅有一例,就是2005年FDA批准用于肾癌治疗的索拉非尼(Sorafenib)[7]。另一方面,来源于自然界的天然产物,其结构经过了长期的自然选择,它们在药物发现中具有人工合成化合物所不能比拟的优势,因而在药物化学中具有独特而重要的地位[6, 8]。
2 天然产物与药物化学
天然产物(natural product)是生物体产生的次级代谢物(secondary metabolite),均为有机化合物。传统上,天然产物主要从陆生动植物以及微生物发酵液中提取。近半个世纪以来,海洋低等生物如无脊椎动物、藻类、真菌等已成为众多骨架结构新颖复杂、具有重要生理活性的海洋天然产物的来源[9]。本质上,由于生物多样性和地理多样性的存在,天然产物也自然地呈现出多样性,常常具有丰富、新颖、复杂的化学结构,且许多为手性分子。这些丰富多样的结构是天然产物具有多种多样生理活性的物质结构基础。天然产物在药物化学研究中的突出意义在于为药物设计提供灵感、为药物发现提供先导化合物。
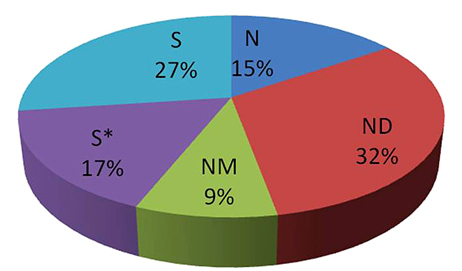
天然产物是药物发现的源泉,在药物化学中占有重要地位。一些化学药物本身就是天然产物,而更多的则是天然产物衍生物、模拟天然产物结构的天然产物类似物以及以天然产物结构为关键药效团的合成药物。据Newman等人的统计,从1981—2006年的25年间,全世界获批准的1 010种用于各种疾病治疗的药物中,化学药物为847种(84%),生物药物含疫苗为163种(占16%)。在化学药物中,与天然产物结构相关的化学药物为537种,占化学药物的63%,具体来看,天然产物(N)占5%;天然产物衍生物(ND)占27%;天然产物类似物(NM)占25%;以天然产物结构为关键药效团的合成药物(S*)占6%;此外310种与天然产物结构不相关的化学合成药物(S)占化学药物的37%(图2)[7]。
染性疾病和癌症的治疗药物中,源于天然产物的药物所占比例更高。Newman的调查表明,从1940—2006年的50多年间,全世界获批准用于癌症治疗的化学药物为155种,与天然产物结构相关的化学药物为113种,所占比例高达73%(图3)。
与天然产物相关的重要药物不胜枚举,如植物来源的鬼臼毒素、石杉碱、芹菜甲素、丹参素、牛膝多糖、柴胡皂甙、薯蓣皂甙、OSW-1等,微生物来源的青霉素、头孢菌素、链霉素、红霉素、橘霉素、万古霉素、雷帕霉素、埃坡霉素、他汀类药物等。我国地域辽阔,各地地理和气候条件有显著差异,天然资源丰富,加之中草药应用具有悠久历史和丰富翔实的典籍记载,并有实力雄厚的天然药物研究队伍和专业机构,因此从事以天然产物为基础的药物化学研究的条件得天独厚。限于篇幅,下面选取数例简要介绍重要天然产物的相关药物化学研究。
3 天然产物药物化学研究实例3.1 青蒿素
首先介绍内过氧 (endoperoxide) 天然产物的研究历史。最早在1912年,首个内过氧天然产物Ascaridole 被分离鉴定,属单萜类化合物。1947年人们分离了另一个内过氧天然产物Ergosterol endoperoxide。由于内过氧天然产物数目极少,相关化学研究和药物化学研究未引起重视。上世纪60年代,前列腺素在一系列重要生化过程中的作用已被揭示,此时高度活泼的含内过氧基团的前列腺素PGH2和PGG2也被分离鉴定并被证明是其他一系列重要前列腺素的生源合成前体[10] 。但真正使人们认识到内过氧天然产物的巨大药用价值的是青蒿素(图4)。
青蒿素及其衍生物作为抗疟特效药是我国科学家对人类抗疟事业做出的杰出贡献。东晋名医葛洪在其名著《肘后备急方》中记载了青蒿绞汁内服可治疟疾。1972年,我国科研人员成功地从青蒿 (Artemisia annua)中分离出青蒿素单体。1976年,我国化学家周维善等人确定了青蒿素的分子结构[11] 。该分子为一独特的内过氧倍半萜,共四个环,其中一个为δ-内酯环,一个为1,2,4-三 烷,分子中共有七个手性中心。1983年,我国化学家周维善、许杏祥等人从青蒿酸出发实现了青蒿素的半合成,1984年实现了全合成,这些工作具有鲜明的接力合成和仿生合成的特点,代表了当时我国有机合成的水平,也为了解青蒿素分子的化学性质和结构改造奠定了基础(图5)[12]。值得一提的是,另一个具有抗疟活性的天然产物鹰爪甲素分子中含有过氧基团这一事实对青蒿素结构鉴定具有启发作用,但其结构确定晚于青蒿素[13]。
作为当今最有效的抗疟药物,青蒿素(及其衍生物)具有高效、速效、低毒、对抗药性恶性疟有效等特点,是救治脑疟等凶险型疟疾的首选药物。结构活性关系研究表明,青蒿素分子中的过氧基团是关键的药效团,用Ph3P或者H2/Pd将过氧基团还原所得的去氧青蒿素即失去抗疟活性。研究表明,过氧基团氧化疟原虫所吞噬的血红细胞中的铁卟啉,产生高活性的自由基物种,破坏疟原虫的消化空泡细胞膜,最终导致疟原虫死亡[14]。但是,青蒿素及其衍生物的详细的抗疟机制在学术界尚未达成共识,如另一种理论就认为疟原虫体内的肌内质网钙三磷酸腺苷酶 (SERCA,钙离子泵)是青蒿素的作用靶点[15]。由于结构特点和作用机制和喹啉类抗疟药物完全不同,青蒿素类药物对氯喹和甲氟喹等无交叉抗药性。值得指出的是,抗疟药物氯喹(Chloroquine)、甲氟喹(Mefloquine)等也都是著名天然抗疟药物奎宁(Quinine)的类似物(图6)。
青蒿素分子只含有C, H, O三种元素,不含N元素,打破了抗疟药物必须含有氮杂环的传统认识,为新型抗疟药物的设计和发展开辟了新天地。以青蒿素为基础,我国科学家又研制出了双氢青蒿素、蒿甲醚、青蒿琥酯等具有更强活性和其他优点的抗疟药物。当今,以青蒿素衍生物为基础的青蒿素联合疗法(ACT)正在拯救疫区亿万民众,为世界范围内的抗疟发挥了不可替代的作用。值得指出的是,在2002年,首个ACT类复方Coartem被添加到WHO的基本药物目录中,从此成为各国应对疫情的首选药物。
今天,关于青蒿素的研究方兴未艾,更多基于青蒿素骨架结构或其过氧药效团的抗疟药物正处在研究的不同阶段,有些已经处在临床试验阶段,如处于二期临床的Artemisone,处于三期临床的Arterolane(代号OZ277,其中OZ表示ozonide臭氧化物,包含过氧基团),以及处于二期临床的代号为OZ439的药物。这些药物为应对可能出现的抗药性疟疾提供了新的选择[16]。此外,青蒿素及其衍生物在抗血吸虫及其他寄生虫,以及抗癌等研究中也取得了令人振奋的结果[17](图7)。
青蒿为一年生草本植物,在我国南北各省均有分布,资源丰富。如今青蒿作为重要的经济作物和战略资源受到特别的重视,但在青蒿素的巨大药用价值被发现以前,作为药材收购的青蒿所占比例极小,大部分仅作为绿肥使用。青蒿素的发现改变了传统药材青蒿的命运,也为如何利用天然药物这一宝库服务于人类健康提供了有益的参考。
3.2 喜树碱
喜树(Camptotheca acuminata)是一种暖地速生落叶乔木,广泛分布于我国长江以南各省低海拔地区,为我国特有树种。1966年Wall和Wani在进行抗癌化合物筛选时发现了天然产物喜树碱 (Camptothecin,CPT,图8)。化学结构上,喜树碱为具有A/B/C/D/E五环骈环结构的生物碱,A/B为喹啉环,C为吡咯环,D为吡啶酮,E为δ-内酯,唯一的手性中心为位于E环的季碳中心C(20),具有 (S)绝对构型,分子近乎平面结构[18]。化学性质方面,喹啉环与吡啶酮环形成大共轭体系,使喹啉氮因受到吡啶酮拉电子效应影响而碱性极弱,因此,喜树碱不能成盐;E环极易水解,在弱碱性条件和中性条件下即水解开环,在酸性条件下较稳定。动物试验表明喜树碱有很强的抗癌活性,但是水溶性差,并伴有较严重的毒副作用。10-羟基喜树碱比喜树碱水溶性好,活性更强,毒副作用相对较轻(图8)。
对喜树碱(CPT)及其衍生物的抗癌活性研究为人们揭示了新颖的作用机制,即CPT通过抑制DNA拓扑异构酶I(Topo I)而达到抗癌作用。Topo I 普遍存在于原核与真核细胞的细胞核内,催化DNA链的断裂和结合,从而控制DNA的拓扑状态,对维持DNA 的超螺旋和DNA复制、转录、重组等多种细胞过程至关重要。Topo I与DNA通过共价键形成可逆复合物,CPT可通过氢键结合到该可逆复合物上,形成三元复合物,从而稳定了上述可逆复合物,这种稳定化作用使DNA复制过程被扰乱,最终导致细胞凋亡。CPT的近平面结构在三元复合物的形成中是重要因素,而氢键的形成则与E环的羟基和内酯以及D环的羰基有关。C(20)手性中心的(S)构型对CPT的抗癌活性至关重要,若为 (R)构型或将羟基还原成氢都失去活性[19]。
喜树碱的全合成一直受到有机合成化学家的关注,我国学者在这个领域也颇有作为[20]。图9为最近姚祝军等人的不对称全合成概要,合成路线采用了有机催化、杂DA反应、金属催化等方法学,总产率达16%,对映体过量为95%。
关于喜树碱的化学结构改造已进行了大量的研究[21]。在某些位置引入合适的取代基可增强对Topo I的抑制活性,改善水溶性,提高E环稳定性和降低毒副作用。其中,A/B环的C(7)、C(9)、C(10)、C(11)是研究最多的结构修饰部位,已上市的抗癌药物10-羟基喜树碱、拓扑替康(Topotecan)、伊立替康(Irinotecan)等均是在这些位置进行结构修饰的产物(图 10)。另一个改造点位于E环。C(20) 羟基被氢、卤素、烷基取代后活性明显下降,环上氧原子用碳、氮、硫等其他原子取代导致活性消失。目前比较成功的改造方式在于稳定内酯结构,因为内酯开环使活性大大降低,毒副作用增加。一类改造是将C(20) 羟基酯化,如已进入临床二期的Afeletecan。还有一类是将E环扩环成七员内酯环,如已进入临床二期的Diflomotecan(图 10)。
3.3 紫杉醇
1967年Wall和Wani报道了分离自太平洋紫杉(Pacific yew,学名短叶紫杉Taxus brevifolia,又名红豆杉)树皮中的一种天然产物对白血病细胞和肿瘤细胞有很强的抑制活性,并将其命名为紫杉醇(Taxol,图11)。1971年,他们又通过X射线单晶衍射确定了紫杉醇独特的分子结构,其核心为一种极复杂的四环二萜,一条具有β-氨基-α-羟基酸结构的边链以酯键与该核心的13-羟基连接,形似该分子的“尾巴”;分子共有11个立体中心,4个季碳,1个四取代双键[22]。1979年,Horwitz发现紫杉醇抑制癌细胞的新机制,即干扰细胞中微管的正常解离[23]。微管 (microtubule) 是组成细胞骨架的部件,其本身是由两种微管蛋白 (α-tubulin, β-tubulin) 的二聚体聚合而成。微管的形成与解聚对维持细胞多种正常功能至关重要,这些功能包括细胞分裂、细胞形态保持、大分子细胞内移动等等。与一些抗癌药物如秋水仙碱通过阻碍微管蛋白聚合成微管从而产生细胞毒性不同,紫杉醇通过稳定微管、抑制微管解离而导致细胞凋亡。这种新机制的发现激发了科学界广泛的研究兴趣。
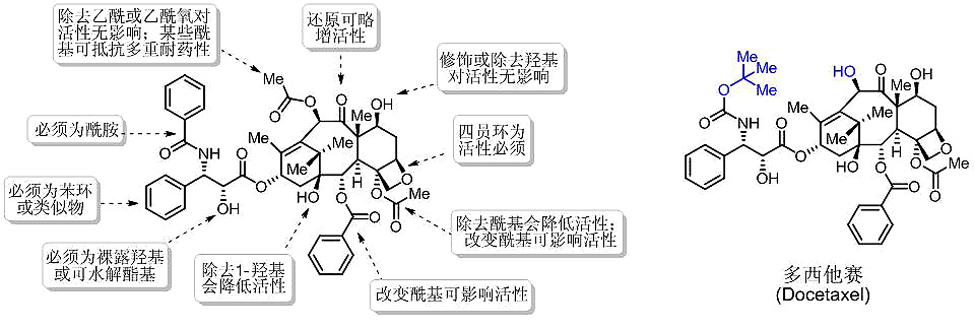
1992年,FDA批准紫杉醇注射液上市,用于治疗卵巢癌、乳腺癌及非小细胞肺癌。结构改造物多西他赛 (Docetaxel) 比紫杉醇水溶性好,活性更强,在2004年FDA批准其用于前列腺癌和乳腺癌的治疗,2006年又批准其用于胃癌和头颈癌的治疗。紫杉醇构效关系的研究比较充分,如图11所示。
紫杉醇在紫杉中的含量约为万分之一,每生产1 kg紫杉醇纯品相当于砍倒2 000多棵百年以上树龄的红豆杉!因此如何在不破坏生态环境的前提下大量获取紫杉醇是当时亟待解决的问题。这一难题的存在,加之全合成方面的挑战性,引起了国际上众多有机合成小组的强烈兴趣,数十个小组先后从事了紫杉醇的合成研究,盛况空前。1989年,佛罗里达州立大学的Robert A. Holton以从欧洲紫杉(Taxus baccata)叶中可较大量提取的10-脱乙酰巴卡廷III (10-DAB III)为原料,完成了紫杉醇的实用性半合成。1994年,Holton小组又率先实现了紫杉醇的首次全合成[24]。此后,Nicolaou(1994)、Danishefsky(1996)、Wender(1997)、Kuwajima(1998)、Mukaiyama(1998)等小组各自以不同策略相继完成了紫杉醇的全合成。Holton的半合成法为紫杉醇的大量供给问题提供了有效解决方案,而这些全合成研究本身也促进了有机合成化学的发展。百时美施贵宝公司采用的紫杉醇半合成路线如图12所示,由10-DAB-III与Ojima内酰胺(Ojima lactam)进行组装。
令人遗憾的是,尽管技术上的难题已经突破,但是只追求眼前经济利益而忽视生态福利和可持续发展的悲剧还是在我国部分地区持续了多年。调查显示,1992—2001年的近10年间,我国云南部分地区红豆杉资源几乎被消耗殆尽,上百万株野生红豆杉惨遭剥皮的命运,对当地生态造成严重破坏[25]。应坚决杜绝此类悲剧的再次发生。
4 结语
本文通过青蒿素、喜树碱、紫杉醇等药物研究概况管窥天然产物在药物发现中的重要性。天然产物是大自然对人类的馈赠,为人类的健康幸福发挥着不可替代的作用。现有化学药物超过半数发源于天然产物,而在抗癌药物中更是超过2/3发源于天然产物。地球上物种极其丰富多样,迄今人类所研究过的物种和天然产物只占自然界存量的极小部分,绝大部分仍属未知,因此需要大大强化天然产物分离、鉴定、活性测试方面的研究,以发现更多的药物或先导。另一方面,需要加强天然产物合成研究和药物化学研究,这是药物发现和最终工业化生产的基础。最后,天然产物作为药物发现持久、可靠的源泉,在根本上要求加大生态环境保护力度,实现人与自然和谐共存,使生物多样性能够持续。